問題詳情
【題組】34.( )化石燃料是現今地球上最主要的能源,一般火力發電廠利用燃燒反應,將化學能轉變為熱能,用來推動發電機以產生電能。但是使用這種方式,最有效率的發電廠也僅能轉換約40%的化學能為電能。若能利用電化學方法,直接將化學能轉變為電能,將更有效率,燃料電池即以此種方式產生電能。氫—氧燃料電池與甲烷燃料電池所需半反應的標準還原電位如下:O2(g)+4H+(aq) + 4e–→2H2O(
(A)每產生1.0莫耳的水,兩種電池都需要轉移2.0莫耳的電子
(B)甲烷燃料電池的電動勢為1.40 V
(C)氫—氧燃料電池的電動勢為1.23 V
(D)燃料電池的能量轉換效率比傳統發電機高
(E)燃料電池的燃料選擇性非常高,除了純氫氣、烷以外,也可運用甲醇、乙醇做為燃料電池的燃料
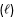
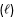
(A)每產生1.0莫耳的水,兩種電池都需要轉移2.0莫耳的電子
(B)甲烷燃料電池的電動勢為1.40 V
(C)氫—氧燃料電池的電動勢為1.23 V
(D)燃料電池的能量轉換效率比傳統發電機高
(E)燃料電池的燃料選擇性非常高,除了純氫氣、烷以外,也可運用甲醇、乙醇做為燃料電池的燃料
參考答案
答案:[無官方正解]
難度:適中0.5
統計:A(0),B(0),C(0),D(0),E(0)
難度:適中0.5
統計:A(0),B(0),C(0),D(0),E(0)