問題詳情
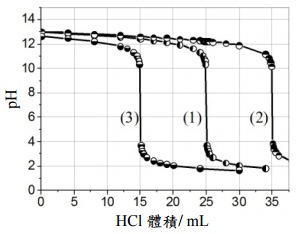
二、甲、乙、丙、丁四瓶溶液,分別含有氫氧化鉀(KOH)、氫氧化鈣(Ca(OH)2)、鹽酸(HCl)與硫酸(H2SO4),但因標籤脫落,無法識別。根據下列分析結果,回答問題⑴至⑷: ⑴從甲瓶溶液中取出 25.00 mL,再以標準 HCl 溶液滴定,所得的結果如下圖中的滴定曲線(1)。 ⑵另從甲瓶溶液中取出 25.00 mL,再加入 10.00 mL 濃度為 0.100 M 的 KOH。充分混合後,以同一 HCl 溶液滴定,所得的結果為曲線(2)。 ⑶另從甲瓶溶液中取出 25.00 mL,再從乙瓶溶液中取出 10.00 mL 溶液,充分混合後,再以同一 HCl 溶液滴定,所得的結果為曲線(3)。 ⑷對步驟⑶的混合液進行分析,發現滴入草酸銨,溶液無明顯變化,但滴入氯化鋇,則出現白色沉澱。
【題組】⑴標準 HCl 溶液的濃度為多少 M?詳述計算過程。(5 分)
【題組】⑴標準 HCl 溶液的濃度為多少 M?詳述計算過程。(5 分)