問題詳情
48. 對某KMnO4標準溶液的濃度進行標定時,先將0.2010公克的草酸鈉(Na2C2O4) 置於錐形瓶中、加入 50.00 毫升 1 M 硫酸水溶液酸化並搖晃使草酸鈉完全溶解後,再將此水溶液加熱至 60 ℃,趁熱以此KMnO4標準溶液滴定,當滴入 25.00 毫升時,恰到達滴定終點。接著另以此KMnO4標準溶液滴定某含有亞鐵離子 (
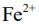
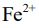
(A) 33.60
(B) 67.20
(C) 134.4
(D) 168.0
參考答案
答案:C
難度:計算中-1
書單:沒有書單,新增
難度:計算中-1
書單:沒有書單,新增