問題詳情
6.pKa可由log Ka =
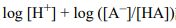
(A)
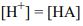
(B)
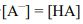
(C)
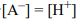
(D)
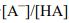
參考答案
答案:B
難度:簡單0.7
書單:沒有書單,新增
難度:簡單0.7
書單:沒有書單,新增
用户評論
【terminator812】評論
B的時候log1=0所以那個公式log Ka = Ka=log[H+]
【鐵觀音鮮奶茶 無去】評論
logKa = log [H+] + log[ A- ] / [ HA ],何時pKa = pH- log [H+] =pHpKa = pH,- log [H+] =-logKa代表logKa = log [H+] + 0log10 [ A- ] / [ HA ] =010丟過去,10 0 = 1, [ A- ] / [ HA ] =1 [ A- ] = [ HA ]
【鋼槍小企鵝】評論
By 企鵝藥分 &n........
【ching】評論
pKa = pH → log Ka=log[H+] log Ka=log[H+]+log([A-]/[HA]) log Ka-log[H+]= 0 =log([A-]/[HA])=log 100=log1 得 : [A-]=[HA] → (C)
【備考不要一律死背,盡量理解】評論
補充個其他題目的迅速判斷方法,由於本人極討厭背Henderson方程式,這個公式背錯酸鹼就是一體兩面的事,因此推薦圖像記憶法,可以看到不管酸還是鹼性藥物,都可以記:越往中間ph值靠,兩者都傾向於離子化