問題詳情
16-17 題為題組
有甲、乙、丙、丁、戊、己 等六個前三週期的元素,其相關的性質如表 3 所示。
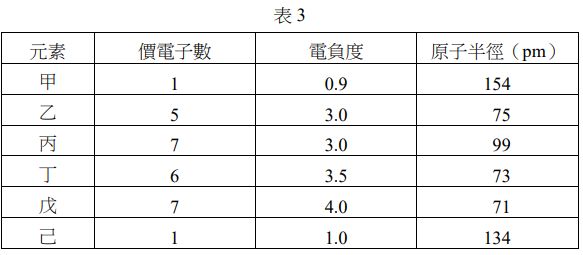
【題組】16.根據表3所提供的資料,下列有關此六個元素的敘述哪些正確?
(A)室溫下,甲可與甲醇反應
(B)乙的第一游離能小於丁的第一游離能
(C)室溫下,丙分子會與水進行氧化還原反應,而丁分子則不會
(D)丁可形成雙原子和三原子兩種氣體分子,其中三原子分子的鍵長較長
(E)室溫下,丙和戊均可形成同核雙原子分子,且戊分子的沸點比丙分子的沸點高
參考答案
答案:ACD
難度:計算中-1
書單:沒有書單,新增
難度:計算中-1
書單:沒有書單,新增
用户評論
【Kai】評論
利用表中資訊先推論各個元素是誰:首先由電負度可以很準確地抓到EN=4的戊為F。而與戊相同價電子數,且EN稍小,原子半徑較大的丙為Cl。以此類推,乙、丁為EN稍小,原子半徑稍大的同週期元素N、O。剩下的甲、己不是H,為IA族的Na、Li。(A)正確。(B)錯誤。N的p軌域半滿較穩定,第一游離能乙>丁。(C)正確。氯氣可以、氧氣不行。(D)正確。可形成O2與O3,其中氧氣鍵級=2,臭氧則為1.5。因此三原子分子的鍵長較長。(E)錯誤。可形成Cl2與F2,比較沸點時看電子總數可知為丙>戊。