問題詳情
31. 已知氮氣與氧氣反應生成二氧化氮的平衡反應式如下:
(A)此反應為一放熱反應
(B)二氧化氮的莫耳生成熱為68 kJ
(C)此反應式符合質量守恆定律
(D)此反應中氮氣扮演氧化劑的角色
(E)二氧化氮溶於水後,可使藍色石蕊試紙變成紅色
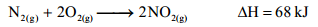
(A)此反應為一放熱反應
(B)二氧化氮的莫耳生成熱為68 kJ
(C)此反應式符合質量守恆定律
(D)此反應中氮氣扮演氧化劑的角色
(E)二氧化氮溶於水後,可使藍色石蕊試紙變成紅色
參考答案
答案:C,E
難度:困難0.25
統計:A(2),B(3),C(1),D(0),E(2)
難度:困難0.25
統計:A(2),B(3),C(1),D(0),E(2)
用户評論
【鄭雅方】評論
A 由 N2(g)+2O2(g) → 2NO2(g),△H=68 kJ,因反應熱為正值,故為吸熱反應。B 1/2N2(g)+O2(g)→ NO2(g) △H=34 kJ 二氧化氮的莫耳生成熱應為 34 kJ。C 化學反應一定遵守質量守恆定律。D 此反應過程中,氮氣被氧化為二氧化氮,故扮演還原劑的角色,而氧氣扮演氧化劑的角色。E 二氧化氮溶於水後會發生反應生成硝酸: 3NO2(g)+H2O(A) → 2HNO3(aq)+NO(g),故可使藍色石蕊試紙變成紅色。