問題詳情
17. 太空載具常以氫氧化鋰吸收太空人所呼出的二氧化碳,其反應式如下:
(A) 0.108
(B) 0.538
(C) 3.20
(D) 6.50
(E) 32.0
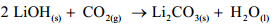
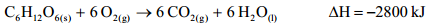
(A) 0.108
(B) 0.538
(C) 3.20
(D) 6.50
(E) 32.0
參考答案
答案:D
難度:適中0.447368
統計:A(1),B(10),C(12),D(34),E(3)
難度:適中0.447368
統計:A(1),B(10),C(12),D(34),E(3)
用户評論
【鄭雅方】評論
已知太空人平均每天所消耗的能量為 3000 大卡,則執行任務 5 天共消耗能量=3000*5*4.2=6.3×10000(千焦)由 C6H12O6(s)+6O2(g)→ 6CO2(g)+6H2O △H=-2800 千焦,可知每莫耳葡萄糖氧化,可放熱2800 千焦,同時生成 6 莫耳 CO2 2800÷6=6.3×10000÷n,n=135,即執行任務 5 天共生成 135 莫耳 CO2。 再由 2LiOH(s)+CO2(g) → Li2CO3(s)+H2O(l),可知 2 莫耳 LiOH 可吸收 1 莫耳 CO2,則 135 莫耳 CO2 需要 270 莫耳 LiOH,才能完全被吸收,其質量為 270×23.9=6453g=6.453kg