問題詳情
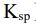
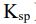
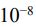
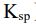
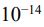
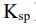
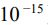
(A) AB>A3B>AB2
(B) AB>AB2 >A3B
(C) A3B>AB2 >AB
(D) AB2 >A3B>AB
參考答案
答案:A
難度:計算中-1
書單:沒有書單,新增
難度:計算中-1
書單:沒有書單,新增
用户評論
【辛辛】評論
溶度積常數是沉澱的溶解平衡常數,溶度積的大小反映難溶電解質的溶解能力對於溶解平衡 MmAn ⇌ mMn+(aq) + nAm-(aq),其溶度積Ksp = [Mn+]m · [Am-)]n例如,氯化銀(AgCl)的溶解平衡為:AgCl(s) ⇌ Ag+ + Cl-,則 Ksp =[Ag+]·[(Cl-)先寫出反應式AB->A+ + B- 溶解度S1, Ksp=[A+][B-]=S1⋅S1=4*10-8 S1=2*10-4AB2->A+ + 2B- 溶解度S2, Ksp=[A+][B-]2=S2⋅(2S2)2=3.2*10-14 4S23=3.2*10-14 S2=2*10-5A3B->3A+ + B- 溶解度S3, Ksp=[A+][B-]2=(3S3)3⋅(S3) =2.7*10-15 27S34=2.7*10-15 S3=10-4S1>S3>S2 AB > A3B > AB2