問題詳情
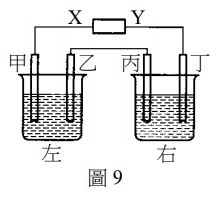
23.某一電解槽的示意圖如圖 9 所示。左燒杯中裝有 100 毫升 0.50 M 的硝酸銀(AgNO3)溶液,右燒杯中裝有 100 毫升 0.25 M 的氯化銅(CuCl2)溶液;甲、乙、丙及丁為質量相同的石墨電極,X 與 Y 為直流電源的兩極。電解一段時間後,甲電極比其他三個電極重。下列敘述,哪些正確?
(A)直流電源的X為陰極,Y為陽極
(B)電解後,左燒杯溶液的pH小於7
(C)甲電極進行還原反應,析出Ag
(D)電解後,僅左燒杯產生氣體
(E)丙電極進行還原反應,析出物的莫耳數為甲電極析出物的一半
參考答案
答案:B,C,E
難度:非常困難0
書單:沒有書單,新增
難度:非常困難0
書單:沒有書單,新增
用户評論
【Kai】評論
(C)首先,甲有變重的話可以代表說他在這個系統當中的角色為陰極,進行的是還原反應,析出Ag。(A)由甲的推論可知,X為陽極,Y為陰極。(B)(D)左燒杯除了進行還原Ag的還原半反應之外,在電極乙上還有水的氧化半反應:H2O(l)→2H+(aq)+1/2O2(g)+2e-因此溶液pH會降低,且有氣體產生。但是右邊的燒杯中陽極的氧化半反應也會有氯氣產生,故B選項正確,D選項錯誤。(E)甲電極析出物為Ag,丙電極則為Cu。根據二者的還原半反應:Ag+ + e- → AgCu2+ + 2e- → Cu當二者的電子莫耳數變化相同時,丙電極析出物的莫耳數為甲電極析出物的一半。