問題詳情
3.有一單質子弱酸(HX)的鈉鹽NaX,已知0.50M的NaX溶液之pH值為10.0。現擬以HX和NaX混合配製pH值為6.0的緩衝溶液,則此緩衝溶液中
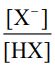
(A)0.20
(B)0.50
(C)1.0
(D)2.0。
參考答案
答案:B
難度:計算中-1
書單:沒有書單,新增
難度:計算中-1
書單:沒有書單,新增
用户評論
【Kai】評論
利用Henderson–Hasselbalch equation:pH = pKₐ + log([A⁻]/[HA])且透過「0.50M的NaX溶液之pH值為10.0」,可先求得Ka=10^-14/(10^-8/0.5)=5 x 10^-7比值即為10^[6-(7-log5)]=10^(-0.3)=0.5